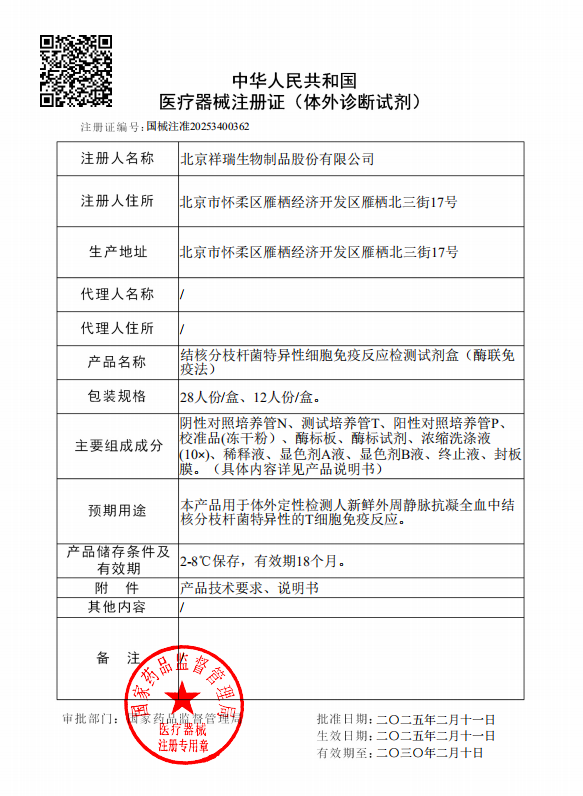
2025 年 2 月 11 日,北京先声祥瑞生物制品股份有限公司自主研发的Ⅲ类结核体外诊断试剂 Xi01 产品(结核分枝杆菌特异性细胞免疫反应检测试剂盒(酶联免疫法))正式获国家药品监督管理局(NMPA)颁发的医疗器械注册证。这是公司打造结核诊疗一体化解决方案服务商的关键突破。Xi01因其高灵敏度和特异性,可为结核病的早期筛查和精准诊断提供可靠支持。
此次获批为 Xi01 产品打开上市通路,使其能快速投入结核病防控工作,成为医疗体系中的有效诊断工具。作为中国结核病诊治领域的创新企业,先声祥瑞长期专注技术研发,始终将推动结核病防治技术进步作为核心战略,持续投入资源深耕。
未来,先声祥瑞将继续以科技创新为驱动,合理规划布局。一方面,公司将针对性地优化产品性能,持续迭代升级,提升用户满意度;另一方面,稳步加大研发投入,拓展产品线,构建更为完善、高效的结核病诊疗体系。通过持续努力,公司旨在为中国抗击结核病持续赋能,向 “终结结核病流行” 的目标扎实迈进,切实履行 “让患者早日用上更有效药物” 的企业使命。
先声祥瑞
先声祥瑞是先声集团旗下成员企业,位于北京雁栖湖畔、怀柔科学城内,是一家正在成为创新驱动型的国家高新技术企业、北京市专精特新“小巨人”企业、北京市企业技术中心。公司集研发、生产、销售预防用生物制品、生物药、化学药、体内及体外诊断试剂为一体,聚焦抗感染、传染病、疫苗领域,全面打造“结核领域一体化解决方案的服务商”,以“致力创新疫苗,造福人类健康”为目标,不断努力前行!
更多信息请访问:www.sanroadbio.com